[Dyne 28th 기초실험방] Two-dimensional(2D) electrophoresis
페이지 정보
작성자 다인바이오 작성일15-02-24 13:35 조회16,800회 댓글0건첨부파일
-
 28_실험자료실_2d electrophoresis..pdf
(381.6K)
5765회 다운로드
DATE : 2016-09-01 14:40:21
28_실험자료실_2d electrophoresis..pdf
(381.6K)
5765회 다운로드
DATE : 2016-09-01 14:40:21
관련링크
본문
Two-dimensional(2D) electrophoresis를 하는 이유는 일반적으로 두 가지로 나누어진다. 첫 번째는 cell이나 tissue에 identification을 이용하여 어떠한 단백질들이 발현되는지를 보는 것이고 두 번째가 그 양의 변화를 보는 것이다. 주로 약물을 투여할 때 나타나는 변화를 보기 위하여 사용하는 경우가 많다. 현재에는 재현성의 문제를 극복하기 위해 DIGE같이 형광 dye를 각 단백질 sample에 염색하여 하나의 gel에서 2개 이상의 sample분석하는 방법도 개발이 되어있으며 phosphorylation, glucosylation등의 특정 signal만을 detect하는 기술들도 발전하고 있다.
2. 2D electrophresis 개념
2D electrophoresis의 가장 큰 개념은 단백질을 2가지 조건으로 나눈다는 것입니다. 그 첫 번째는 pI 즉 등전점으로 단백질을 나누는 것이고 그 다음은 단백질의 분자량으로 나누는 것이다. 등전점으로 단백질을 나누는 것이 first dimension이고 분자량으로 나누는 것이 second dimension 이다.
1) 1D
pI 값으로 단백질을 나누는 것은 단백질상의 카르복실기(-COOH)와 아미노기(- NH2)에 의하여 단백질 전체의 net charge가 pH에 따라 변하는 성질을 이용한 것이다. 분리하고자 하는 단백질을 strip에 loading 한 후 양쪽에 전압을 걸어주면 단백질마다 가진 net charge에 의하여 net charge가 0인 곳으로 이동하게 된다. 산성 쪽에는 (+)charge를 염기성 쪽에는 (-)charge를 걸어주면 다음의 그림과 같이 단백질들이 이동하게 되고 이로 인해 등전점에 따라 분리가 되는 것이다.
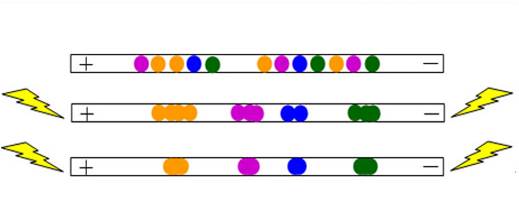
2) 2D
3. 실험방법
1) 단백질의 분리:2D-electrophoresis
모든 단백질들은 구성하고 있는 amino acid에 따라 질량 과 pI(isoelectric point)값이 다르다. 따라서 이 두 요인을 이용하여 단백질을 분리할 수 있다. pI를 이용하여 단백질을 펼치는 방법을 IEF(isoelectric focusing)라고하며 질 량에 의해서 단백질을 펼치는 방법을 SDS-PAGE(SDSpolyacrylamide gel electrophoresis)라고 한다.
2) Sample preparation
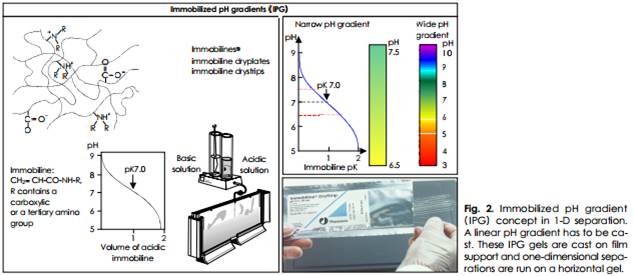
단백질을 pI값에 의해 펼치는 방법으로 1975년 O’Farrell에 의해서 개발되었다. Immobilized pH Gradient (IPG) 라는 개념이 도입되어 immobiline이라는 zwitter ion을 이용 pH gradient를 규칙적으로 생성한다(Fig. 2). 요즈음 IPG gel strip이 상품화되어 재현성이 증가되었다(Figs. 3 and 4).


5) Staining
Gel 안에서 구현된 단백질의 spot을 염색하는 방법으로 silver staining(detection limit 0.5~1.2 ng)과 commassie stain(detection limit 8~26 ng), SYPRO Orange 또는 SYPRO Ruby stain(detection limit 2~10 ng)을 사용한다.
염색된 gel을 스캔하여 image file로 전환하는 과정으로 GS-800 Calibrated Imaging Densitometer, Fluor-S MAX MultiImage System, Molecular Imager FX 등을 사용한다.
7) Image analysis
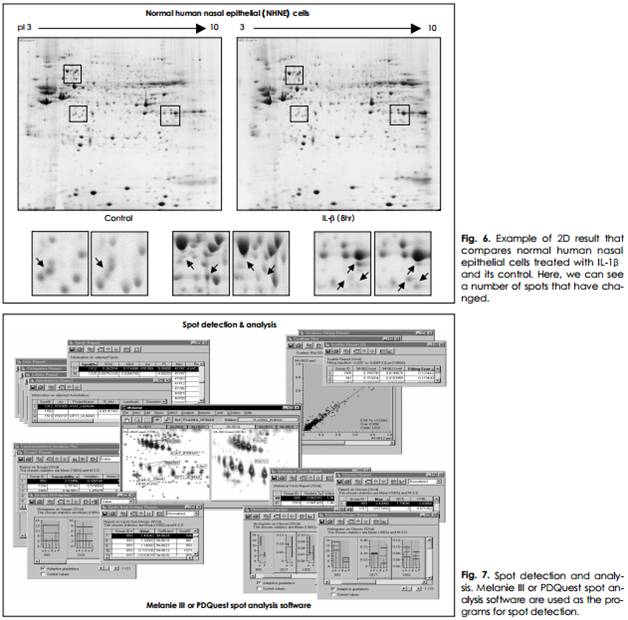
기능성 측면에서는 세포내 단백질의 생리상태별(예, 암과 정상조직) 발현차이와 세포내 상태별 특정단백질의 정량적 차이 및 변형상태, 그리고 상호관계 등을 규정하는데 긴요하다. 활용성 측면에서는 각종 질환 표지자(disease marker)와 치료표적 단백질의 발굴과 동식물성장조절단백질의 규명, 생식기전 및 약물독성과 신의약 개발을 들 수 있다.
- 유전단백체 기능제어 연구센터/건국대학교
- 프로테오믹스, Korean J Otolaryngol 2004;47:705-13/김창훈
